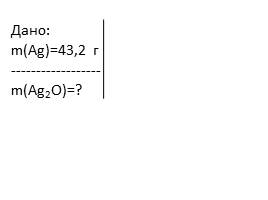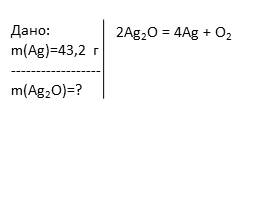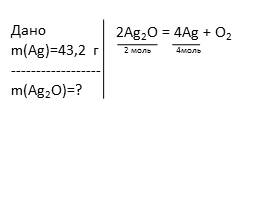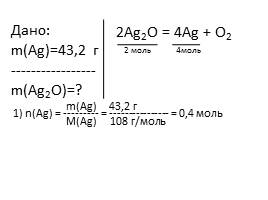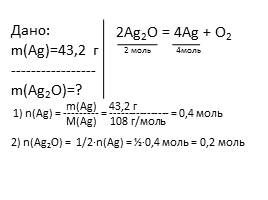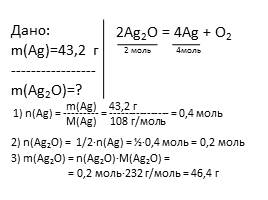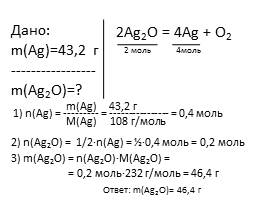Текст этой презентации
Слайд 1

Алгоритм решения задач по химическим уравнениям
Мариинск МБОУ «СОШ №6»
учитель химии, Сарина Татьяна Васильевна
Слайд 2
Слайд 3

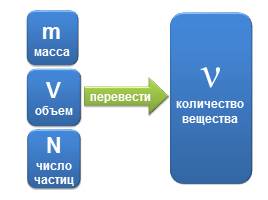
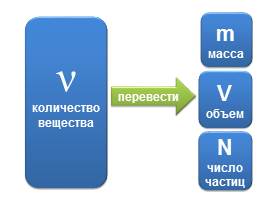
Сравнить количества веществ, участвующих в реакции aA + bB = cC + dD
Слайд 4
Слайд 5

ЗАДАЧА
При нагревании оксида серебра (I) образовалось 43,2 г серебра и кислород. Какова масса разложившегося оксида?
Слайд 6
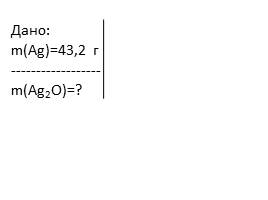
Дано:�m(Ag)=43,2 г�------------------�m(Ag2O)=?
Слайд 7
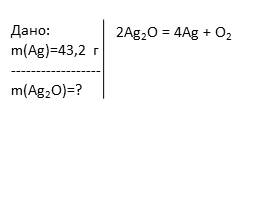
Дано:�m(Ag)=43,2 г�------------------�m(Ag2O)=?
2Ag2O = 4Ag + O2
Слайд 8
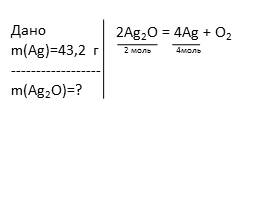
Дано�m(Ag)=43,2 г�------------------�m(Ag2O)=?
2Ag2O = 4Ag + O2
2 моль
4моль
Слайд 9
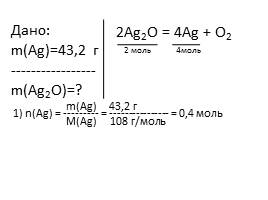
Дано:�m(Ag)=43,2 г�-----------------�m(Ag2O)=?
2Ag2O = 4Ag + O2
2 моль
4моль
1) n(Ag) = --------- = ---------------- = 0,4 моль
m(Ag) 43,2 г
M(Ag) 108 г/моль
Слайд 10
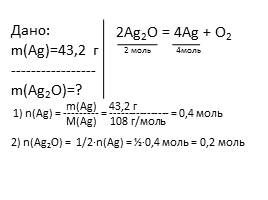
Дано:�m(Ag)=43,2 г�-----------------�m(Ag2O)=?
2Ag2O = 4Ag + O2
2 моль
4моль
1) n(Ag) = --------- = ---------------- = 0,4 моль
m(Ag) 43,2 г
M(Ag) 108 г/моль
2) n(Ag2O) = 1/2∙n(Ag) = ½∙0,4 моль = 0,2 моль
Слайд 11
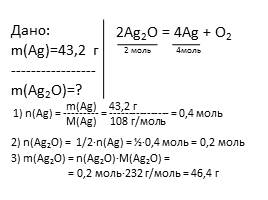
Дано:�m(Ag)=43,2 г�-----------------�m(Ag2O)=?
2Ag2O = 4Ag + O2
2 моль
4моль
1) n(Ag) = --------- = ---------------- = 0,4 моль
m(Ag) 43,2 г
M(Ag) 108 г/моль
2) n(Ag2O) = 1/2∙n(Ag) = ½∙0,4 моль = 0,2 моль
3) m(Ag2O) = n(Ag2O)∙M(Ag2O) = = 0,2 моль∙232 г/моль = 46,4 г
Слайд 12
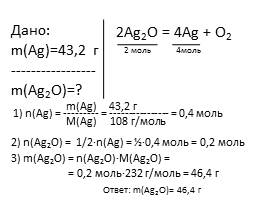
Дано:�m(Ag)=43,2 г�-----------------�m(Ag2O)=?
2Ag2O = 4Ag + O2
2 моль
4моль
1) n(Ag) = --------- = ---------------- = 0,4 моль
m(Ag) 43,2 г
M(Ag) 108 г/моль
2) n(Ag2O) = 1/2∙n(Ag) = ½∙0,4 моль = 0,2 моль
3) m(Ag2O) = n(Ag2O)∙M(Ag2O) = = 0,2 моль∙232 г/моль = 46,4 г
Ответ: m(Ag2O)= 46,4 г
 Первоначальные химические понятия
Первоначальные химические понятия
 Скорость химических реакций
Скорость химических реакций
 Химический состав, строение и функции клеточных мембран - Транспорт веществ через мембрану
Химический состав, строение и функции клеточных мембран - Транспорт веществ через мембрану
 Скорость химической реакции
Скорость химической реакции
 Гидролиз солей
Гидролиз солей