Текст этой презентации
Слайд 1

8 класс
Учитель химии и биологии Абовян Г.М.
МБОУ Свердловская СОШ им. М.П. Марченко
ПРОСТЫЕ ВЕЩЕСТВА -НЕМЕТАЛЛЫ
Слайд 2

НЕМЕТАЛЛЫ - химические элементы, которые образуют в свободном виде простые вещества, не обладающие физическими и химическими свойствами металлов.
Слайд 3

Цели:
Обобщить и систематизировать знания о неметаллах
Уметь характеризовать элементы по положению в периодической таблице
Знать физические и химические свойства
Слайд 4
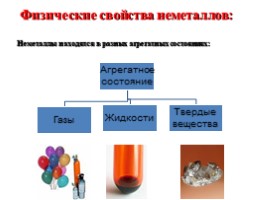
Физические свойства неметаллов: Неметаллы находятся в разных агрегатных состояниях:
Слайд 5

Газообразные вещества неметаллы N2 Не
О2 - Ne
H2 - Ar
Cl2 - Kr
F2 - Xe о3-- Rn Азот, кислород, водород и инертные газы газы-бесцветные, хлор-имеет желто зеленый цвет, фтор светло желтый, озон голубой цвет.
Слайд 6

Твердые вещества:�
S P I2 C Si
сера
фосфор
йод
углерод
Si - кремний
Слайд 7

Жидкое вещество:
бром
Слайд 8

Физические свойства
Не имеют металлического блеска(искл. крист. Йод и графит);
Хрупкие в твердом состоянии; не обладают пластичностью.
Не проводят эл. ток (искл. графит, кремний и черный фосфор обладают полупроводниковыми свойствами);
Различны по окраске.
В воде неметаллы нерастворимы или малорастворимый.
Слайд 9
O3 - озон
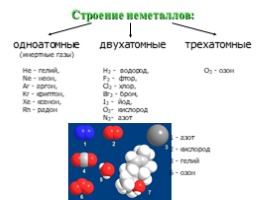
Строение неметаллов:
одноатомные (инертные газы)
двухатомные
трехатомные
He - гелий, Ne - неон, Ar - аргон, Kr - криптон, Xe - ксенон, Rn - радон
H2 - водород, F2 - фтор, Cl2 - хлор, Br2 - бром, I2 - йод, O2- кислород N2- азот
1 - азот
2 - кислород
3 - гелий
6 - озон
Слайд 10

АЛЛОТРОПИЯ
Способность атомов одного химического элемента образовывать несколько простых веществ.
Слайд 11

Причины аллотропии:�
Различное число атомов в молекуле; Образование различных кристаллических форм.
Слайд 12

Аллотропия кислорода. Кислород и озон
Слайд 13

Модификации кислорода.
О2- кислород;
бесцветный газ;
не имеет запаха;
плохо растворим в воде;
температура кипения-182,9 С;
устойчивая молекула.
О3 – озон;
газ голубого цвета;
имеет резкий запах;
растворяется в 10 раз лучше, чем кислород;
температура кипения -111,9 С;
не устойчивая молекула.
Слайд 14

Аллотропия фосфора. Красный и белый фосфор
Р (красный фосфор)
(белый фосфор)
Р4
Слайд 15
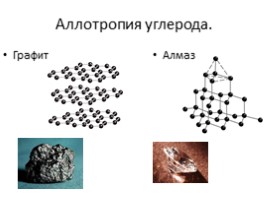
Аллотропия углерода.
Графит
Алмаз
Слайд 16

Аллотропия серы. Кристаллическая, пластическая и моноклинная
Слайд 17

Аллотропия олова
1. B-олово(белое)-представляет собой металл.
При комнатной температуре существует белое олово(В- Sn).
2. a- олово(серое)-серый мелкокристаллический порошок, имеющий свойства неметалла. Процесс превращения белого олова в серое идет при снижение температуры(быстро идет при температуре -33 С.
Слайд 18

Использование неметаллов:
4. Азот N2
топливо в двигателях ракет
азотная кислота
N2
удобрения
взрывчатые вещества
Специальные ткани
Лекарства
Слайд 19
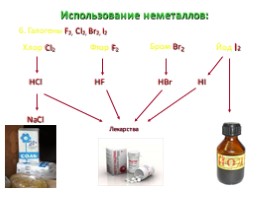
Использование неметаллов:
6. Галогены F2, Cl2, Br2, I2
Хлор Cl2
НCl
NaCl
Лекарства
Фтор F2
НF
Бром Br2
НBr
Йод I2
НI
Слайд 20

Использование неметаллов:
5. Фосфор Р
фосфорная кислота
P
удобрения
Зажигательные вещества
Лекарства
Участие в обмене веществ организмов
Слайд 21

Домашнее задание
П.15,упр. 3.
 Урок-смотр знаний по теме «Изменения, происходящие с веществами» 8 класс
Урок-смотр знаний по теме «Изменения, происходящие с веществами» 8 класс
 Простые и сложные вещества
Простые и сложные вещества
 Вещества и их свойства (8 класс)
Вещества и их свойства (8 класс)
 Чистые вещества и смеси - Способы разделения смесей
Чистые вещества и смеси - Способы разделения смесей
 Своя игра по химии за 8 класс первую четверть
Своя игра по химии за 8 класс первую четверть






















