Презентация - Простые и сложные вещества
просмотров
Текст этой презентации
Слайд 1

Простые и сложные вещества
Мидакова Наталья Васильевна учитель I квалификационной категории
МБОУ «Красночетайская СОШ» Красночетайский район Республика Чувашия
Слайд 2
Содержание
Опорная схема
Алгоритм определения веществ
Проверь себя
Классификация
Строение молекулы
Физические свойства
Простые вещества
Химический словарик
Отличие между сложными и простыми вещ-ми
Классификация
Строение и свойства
Аллотропия
Сложные вещества
Источники
Отличие между сложными вещ-ми и смесями
Приложение
Слайд 3
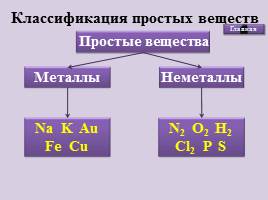
Классификация простых веществ
Простые вещества
Металлы
Неметаллы
Na K Au Fe Cu
N2 O2 H2 Cl2 P S
Главная
Слайд 4
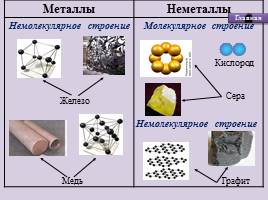
Металлы Неметаллы
Немолекулярное строение Молекулярное строение
Немолекулярное строение
Графит
Кислород
Сера
Медь
Железо
Главная
Слайд 5
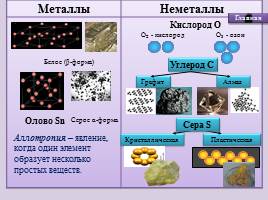
Металлы Неметаллы
Кислород О
Углерод С
Кристаллическая
Пластическая
Олово Sn
Серое α-форма
Белое (β-форма)
Сера S
Главная
Слайд 6
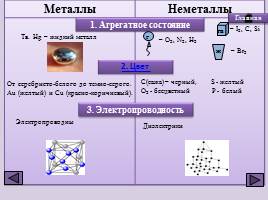
Металлы Неметаллы
1. Агрегатное состояние
Тв. Hg – жидкий металл
– O2, N2, H2
– I2, C, Si
– Br2
2. Цвет
От серебристо-белого до темно-серого. Au (желтый) и Cu (красно-коричневый).
3. Электропроводность
г
тв
ж
Электропроводны
Диэлектрики
Главная
Слайд 7

Металлы Неметаллы
От серебристо-белого до серого
бериллий
германий
литий
золото
графит
мышьяк
алмаз
кремний
сера
фосфор
Главная
медь
Слайд 8

Металлы Неметаллы
4. Твердость / мягкость
Пластичные (Au, Ag, Cu, Al и др.), кроме. Sn (серое).
Хрупкие (S, уголь, I2, др.) При ударе рассыпаются.
5. Пластичность/ хрупкость
Существуют твердые (Cr, Fe) и мягкие (Au, Na, K).
Существуют твердые (Салмаз, Si) и мягкие (Cграфит).
6. Температура плавления
Самая высокая:
Tпл.(W)= +3380°С
Самая низкая?
Tпл.(Hg)= - 38,8°С
Высокая:
Tпл.(алмаза)= +3600°С
Низкая:
Tпл.(азота)= -210°С
Главная
Слайд 9
Главная
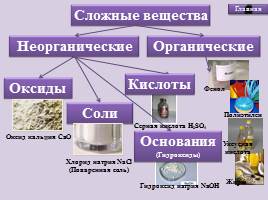
Сложные вещества
Оксиды
Соли
Оксид кальция СаО
Хлорид натрия NaCl
(Поваренная соль)
Кислоты
Гидроксид натрия NaОН
Неорганические
Органические
Основания
(Гидроксиды)
Серная кислота H2SO4
Фенол
Жиры
Полиэтилен
Уксусная кислота
Слайд 10

Сложные вещества состоят из атомов разных химических элементов
В химических реакциях могут разлагаться с образованием нескольких других веществ
Главная
Слайд 11
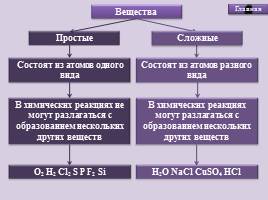
Вещества
Простые
Состоят из атомов одного вида
Состоят из атомов разного вида
В химических реакциях не могут разлагаться с образованием нескольких других веществ
В химических реакциях могут разлагаться с образованием нескольких других веществ
О2 Н2 Cl2 S P F2 Si
H2O NaCl CuSO4 HCl
Главная
Сложные
Слайд 12
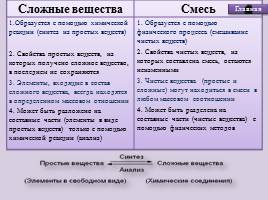
Сложные вещества Смесь
1.Образуется с помощью химической реакции (синтез из простых веществ) 2. Свойства простых веществ, из которых получено сложное вещество, в последнем не сохраняются
3. Элементы, входящие в состав сложного вещества, всегда находятся в определенном массовом отношении
4. Может быть разложено на составные части (элементы в виде простых веществ) только с помощью химической реакции (анализ) 1. Образуется с помощью физического процесса (смешивание чистых веществ)
2. Свойства чистых веществ, из которых составлена смесь, остаются неизменными
3. Чистые вещества (простые и сложные) могут находиться в смеси в любом массовом соотношении
4. Может быть разделена на составные части (чистые вещества) с помощью физических методов
Главная
Слайд 13
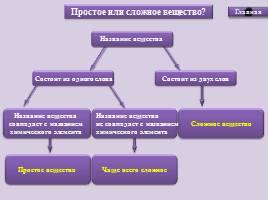
Название вещества
Состоит из одного слова
Состоит из двух слов
Сложное вещество
Название вещества совпадает с названием
химического элемента
Название вещества не совпадает с названием
химического элемента
Простое вещество
Чаще всего сложное
Простое или сложное вещество?
Главная
Слайд 14
Главная
Слайд 15
Ошибка
Ошибка
Ошибка
Молодец
Ошибка
Ошибка
Ошибка
Ошибка
Ошибка
Ошибка
Молодец
Ошибка
Ошибка
Ошибка
Молодец
Хлор
Аммиак
Колодезная вода
Воздух
Лёд
Фосфор
Сера
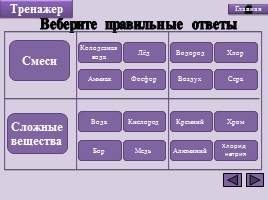
Смеси
Молодец
Сложные
вещества
Вода
Бор
Кислород
Медь
Хлорид натрия
Кремний
Хром
Веберите правильные ответы
Водород
Алюминий
Главная
Тренажер
Слайд 16

Ошибка
Ошибка
Молодец
Ошибка
Состоят из атомов разных химических элементов
Ошибка
Молодец
Ошибка
Ошибка
Имеют аморфные модификации
Ошибка
Ошибка
Ошибка
Молодец
Смесь
Ошибка
Ошибка
Молодец
Ошибка
Простое вещество
Ошибка
Ошибка
Ошибка
Молодец
Сложное вещество
Главная
Тест
Выберите один правильный ответ
Слайд 17
1. http://www.himhelp.ru/section24/section8/section48/
2. http://ru.wikipedia.org/wiki/Простые вещества
3. http://biolabyrinth.narod.ru/chem/general/basic/chem-bas.htm
Главная
4. http://school-collection.edu.ru/catalog/res/c90b7e4a-ece0-1df5-2e83-66ce2d07ae9d/?from=eb17b17a-6bcc-01ab-0e3a-a1cd26d56d67&interface=themcol
5. http://school-collection.edu.ru/catalog/res/0A22315C-8AAD-C506-5565-CB501F201476/?interface=catalog&class=Array&subject=Array
Интернет ресурсы
1. Бочарова С.И. Занимательные материалы по химии. Издательство Корифей; 2. Габриелян О.С. Химия: 8 кл. – М: Дрофа, 2003; 3. Габриелян О.С., Смирнова Т.В. Изучаем химию в 8 классе. – М: БЛИК и К0, 2004; 4. Еремина Е.А., Еремин В.В, Кузьменко Н.Е. Справочник школьника по химии. М. Дрофа, 1996. 5. Рудзитис Г.Е., Фельдман Ф.Г. Химия 9 кл. -М.: Просвещение, 2007
Литература
CD ресурсы
Виртуальная химическая лаборатория. 9 кл. (CD компания «Новый диск»).
Слайд 18
Главная
Приложение
Слайд 19
Простое вещество Tплавл. Простое вещество Tплавл.
Азот
Алюминий
Барий
Бром
Водород
Вольфрам
Железо
Золото -210ºС
660 ºС
767 ºС
-7,2 ºС
-252,6 ºС
3410 ºС
1535 ºС
1064 ºС Иод
Калий
Кальций
Кислород
Кремний
Медь
Ртуть
Сера 113,5 ºС
63,15 ºС
842 ºС
-182,9 ºС
1415 ºС
1084 ºС
-38,9 ºС
112 ºС
№ Название неметалла Химическая формула неметалла Цвет Агрегатное состояние
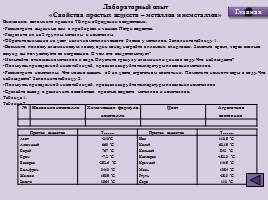
Лабораторный опыт
«Свойства простых веществ – металлов и неметаллов»
Внимание: вспомните правила ТБ при обращении с веществами.
Рассмотрите выданные вам в пробирках и чашках Петри вещества.
Разделите их на 2 группы: металлы и неметаллы
Обратите внимание на цвет, наличие металлического блеска у металлов. Заполните таблицу 1.
Возьмите полоску алюминиевую ложку, один конец нагрейте в пламени спиртовки. Заметьте время, через сколько секунд вы почувствуете ее нагревание. О чем это свидетельствует?
Испытайте отношение металлов к воде. Опустите гранулу алюминия и цинка в воду. Что наблюдаете?
Пользуясь приведенной ниже таблицей, проанализируйте температуры плавления металлов.
Рассмотрите неметаллы. Что можно сказать об их цвете, агрегатном состоянии. Поместите немного серы в воду. Что наблюдаете? Заполните таблицу 2.
Пользуясь приведенной ниже таблицей, проанализируйте температуры плавления неметаллов
Сделайте вывод о различиях в свойствах простых веществ металлов и неметаллов.
Таблица 1.
Таблица 2.
Главная
Слайд 20

Определите местоположение неметаллов в периодической системе.
Неметаллов больше или меньше в периодической системе?
Почему неметаллы относят к простым веществам?
Металлы Металлы Неметаллы Неметаллы
Химический знак Название элемента Химический знак Название элемента
Карточки-задания
Вопросы 1 группе.
При помощи периодической таблицы, ответьте на вопросы:
Вопросы 2 группе.
При помощи периодической таблицы, ответьте на вопросы: Вопросы 3 группе.
Даны следующие химические элементы: Cu, Sn, Au, Ag, Cl, Br, Pb , H, N, Ni, As, He, Fe. 1.Найдите среди них металлы и неметаллы. 2.Укажите название элементов 3.Результаты занесите в таблицу.
Главная
Слайд 21

Главная
Физкультминутка Представьте, что мы высадились на берег, и идем по пустыне. Под ногами зыбучий песок, и мы вязнем в нем по щиколотку. (музыка)
А теперь представьте, что песок нагрелся до такой степени, что ноги просто обжигает, необходимо как можно быстрее пройти этот путь. Музыка.
Опять препятствие, на нашем пути встретились высыхающее болото, но можно замочить ноги. Передвигаемся по кочкам. Скорей, скорей. Музыка.
Вдруг кочки закончились, наши ноги стали вязнуть в болоте, нам трудно передвигаться, но мы справляемся и с этим испытанием. Музыка.
Перед нами река. Давайте посмотрим, что же там за этим мостиком. Идем по деревянному мосту. Ой, он старый, шатается. Осторожно, не упадите в пропасть, держите равновесие.
Музыка. Какая красота. Мы попали в загадочный лес, в котором поют птицы, лес шумит. Можно немного отдохнуть. Звучит тихая музыка.
Молодцы. Открыть страничку с сайта http://priroda.inc.ru/relax/relax24.html с шумом моря. (Включить звук и настроить регуляторы).
Слайд 22
Главная
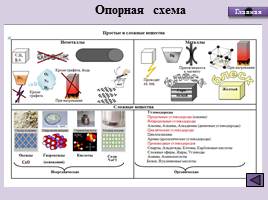
Опорная схема
Слайд 23

Главная
Вариант 1.
1. В химической лаборатории нельзя:
1) проводить опыты;
2) смешивать жидкости;
3) принимать пищу;
4) работать в халате.
2. Жидкости фильтруются с помощью:
1) выпарительной чашки и спиртовки;
2) воронки и фильтровальной бумаги;
3) ступки и пестика;
4) кристаллизатора и стеклянной палочки.
3. Знак химического элемента железо:
1) F; 2) Fе; 3) Gе; 4) Cu.
4. Атомы различных элементов различаются:
1) только по массе;
2) только по цвету;
3) по массе и по цвету;
4) по массе и по объему.
5. Для разделения несмешивающихся жидкостей используют:
1) делительную воронку;
2) обычную воронку;
3) ступку и пестик;
4) круглодонную колбу и холодильник.
Проверка знаний. Тест
Задание. Выберите один правильный ответ.
Слайд 24

6. Вещество – это:
1) стакан; 2) гвоздь;
3) железо; 4) конверт.
7. Смесь представляет собой:
1) вода; 2) сахар;
3) соляная кислота; 4) медь.
8. Моль – это:
1) число частиц, содержащихся в 1 г любого вещества;
2) 1/12 часть массы изотопа углерода 12С;
3) единица измерения физической величины – количества вещества;
4) число молекул, содержащихся в 22,4 л газа при нормальных условиях (н.у.).
9. Если воду добавить к серной кислоте, то:
1) эти жидкости не будут смешиваться;
2) произойдет сильное охлаждение раствора;
3) возможно вскипание и разбрызгивание раствора серной кислоты;
4) серная кислота вступит в реакцию обмена с водой.
10. Химический элемент – это:
1) разновидность атомов;
2) тип вещества;
3) класс молекул;
4) то же, что и простое вещество.
Главная
Слайд 25

Главная
Вариант 2
1. В химической лаборатории можно:
1) употреблять пищу;
2) склоняться для лучшего обзора над приборами при проведении опыта;
3) выливать реактивы в раковину;
4) выполнять опыты согласно инструкции.
2. Вещества в химической лаборатории растирают с помощью:
1) ступки и пестика;
2) стеклянной палочки и кристаллизатора;
3) любых подручных средств;
4) выпарительной чашки и штатива.
3. Знак химического элемента гелий:
1) Ge; 2) He; 3) Ga; 4) Hg.
4. Газообразные вещества, такие, как кислород, азот, водород, состоят из мельчайших частиц, называемых:
1) атомы; 2) молекулы;
3) химические элементы; 4) ионы.
5. Для разделения смешивающихся жидкостей используют:
1) круглодонную колбу, холодильник, приемник, штатив, электрическую плитку;
2) делительную воронку;
3) обычную воронку, фильтровальную бумагу и стакан;
4) плоскодонную колбу, дефлегматор, холодильник, спиртовку, приемник.
Слайд 26

6. Телом является:
1) графит; 2) алмаз;
3) бумага; 4) гвоздь.
7. Смесь, которую можно разделить с помощью магнита:
1) сера и сахар;
2) медь и стекло;
3) песок и мел;
4) медные и стальные опилки.
8. Одинаковые количества вещества (в моль) различных веществ имеют также одинаковую:
1) массу:
2) объем;
3) число структурных единиц;
4) число атомов.
9. Емкости с кислотой вместимостью более 3 л категорически запрещено переносить в:
1) металлическом ведре;
2) руках;
3) корзине с прокладками из поролона или стружек;
4) пластмассовом ведре.
10. Химический элемент – это:
1) то же, что и простое вещество;
2) наименьшая химически неделимая частица;
3) то, из чего состоит вещество;
4) вид атомов.
Главная
Слайд 27

Химический словарик
Аллотропия
Смесь
Простое вещество
Сложное вещество
Химическое соединение
Главная
Слайд 28

Тест
«Простые и сложные вещества»
Образовательный портал «Мой университет» Факультет «Реформа образования»
Мидакова Наталья Васильевна учитель I квалификационной категории
МОУ «Красночетайская СОШ» Красночетайский район Республика Чувашия
Выход
Старт
Слайд 29
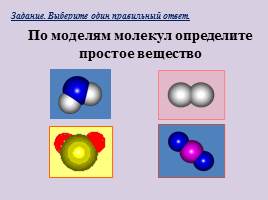
По моделям молекул определите простое вещество
Задание. Выберите один правильный ответ.
Слайд 30
2
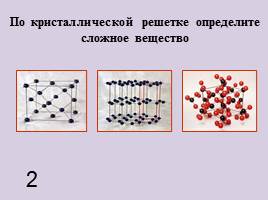
По кристаллической решетке определите сложное вещество
Слайд 31

Выберите простое вещество
1. H2O
2. H2
3. H2O2
4. NH3
0
Слайд 32

1. H2O
2. H2
3. H2O2
4. NH3
1
Выберите простое вещество
Слайд 33

1. H2O
2. H2
3. H2O2
4. NH3
2
Выберите простое вещество
Слайд 34

1. H2O
2. H2
3. H2O2
4. NH3
3
Выберите простое вещество
Слайд 35

1. азот
2. кислород
3. молоко
4. хлор
0
Смесью является:
Слайд 36

1. азот
2. кислород
3. молоко
4. хлор
1
Смесью является:
Слайд 37

1. азот
2. кислород
3. молоко
4. хлор
2
Смесью является:
Слайд 38

1. кислород
2. азот
3. молоко
4. хлор
3
Смесью является:
Слайд 39

1. кислород
2. азот
3. молоко
4. хлор
4
Смесью является:
Слайд 40

1. сложное вещество
2. аллотропия
3. химическое соединение
4. молекула
0
Способность атомов химических элементов образовывать несколько простых веществ с разными свойствами называется
Слайд 41

1. сложное вещество
2. аллотропия
3. химическое соединение
4. молекула
1
Способность атомов химических элементов образовывать несколько простых веществ с разными свойствами называется
Слайд 42

1. сложное вещество
2. аллотропия
3. химическое соединение
4. молекула
2
Способность атомов химических элементов образовывать несколько простых веществ с разными свойствами называется
Слайд 43

1. сложное вещество
2. аллотропия
3. химическое
соединение
4. молекула
3
Способность атомов химических элементов образовывать несколько простых веществ с разными свойствами называется
Слайд 44

1. сложное вещество
2. аллотропия
3. химическое
соединение
4. молекула
4
Способность атомов химических элементов образовывать несколько простых веществ с разными свойствами называется
Слайд 45

1. сложное вещество
2. аллотропия
3. химическое соединение
4. молекула
5
Способность атомов химических элементов образовывать несколько простых веществ с разными свойствами называется
Слайд 46

1. отдельные атомы
2. молекула
3. сложное вещество
4. химическая связь
0
Что изображено на рисунке?
Слайд 47

1. отдельные атомы
2. молекула
3. сложное вещество
4. химическая связь
1
Что изображено на рисунке?
Слайд 48

1. отдельные атомы
2. молекула
3. сложное вещество
4. химическая связь
2
Что изображено на рисунке?
Слайд 49

1. отдельные атомы
2. молекула
3. сложное вещество
4. химическая связь
3
Что изображено на рисунке?
Слайд 50

1. отдельные атомы
2. молекула
3. химическая связь
4. сложное вещество
4
Что изображено на рисунке?
Слайд 51

1. отдельные атомы
2. молекула
3. химическая связь
4. сложное вещество
5
Что изображено на рисунке?
Слайд 52

1. отдельные атомы
2. молекула
3. химическая связь
4. сложное вещество
6
Что изображено на рисунке?
Слайд 53

1. иона
2. сложного вещества
4. молекулы
3. атома
0
Какая модель изображена на рисунке?
водород
Слайд 54

1. иона
2. сложного вещества
4. молекулы
3. атома
1
Какая модель изображена на рисунке?
водород
Слайд 55

1. иона
2. сложного вещества
4. молекулы
3. атома
2
Какая модель изображена на рисунке?
водород
Слайд 56

1 иона
2. сложного вещества
4. молекулы
3. атома
3
Какая модель изображена на рисунке?
водород
Слайд 57

1. иона
2. сложного вещества
4. молекулы
3. атома
4
Какая модель изображена на рисунке?
водород
Слайд 58

1. иона
2. сложного вещества
4. молекулы
3. атома
5
Какая модель изображена на рисунке?
водород
Слайд 59

1. иона
2. сложного вещества
4. молекулы
3. атома
6
Какая модель изображена на рисунке?
водород
Слайд 60

1. иона
2. сложного вещества
4. молекулы
3. атома
7
Какая модель изображена на рисунке?
водород
Слайд 61

Начало
ОТЛИЧНО
Выход
Слайд 62

ХОРОШО
Выход
Начало
Слайд 63
УДОВЛЕТВОРИТЕЛЬНО
Выход
Начало
Слайд 64

ВАША ОЦЕНКА
Выход
Попробуйте снова
Слайд 65

Аллотро́пия (от др.-греч. αλλος — «другой», τροπος — «поворот, свойство») — существование одного и того же химического элемента в виде двух и более простых веществ, различных по строению и свойствам: так называемых аллотропических модификаций или аллотропических форм.
Модификации фосфора
Главная
Слайд 66

Просты́е вещества́ — вещества, состоящие исключительно из атомов одного химического элемента (в отличие от сложных веществ). Являются формой существования химических элементов в свободном виде, или, иначе говоря, элементы, не связанные химически ни с каким другим элементом, образуют простые вещества. Известно свыше 400 разновидностей простых веществ.
Алмаз
Графит
Главная
Слайд 67

Сложные вещества — это химические вещества, которые состоят из атомов двух или более химических элементов. Сложными веществами являются большинство неорганических веществ и все органические.
Вода
Галит
Сильвинит
Главная
Слайд 68

Смесь — Продукт смешения, механического соединения каких-либо веществ. Например: горючая смесь, гелиево-кислородная смесь.
Молоко
Воздух
Главная
Слайд 69

Хими́ческое соедине́ние— сложное вещество, состоящее из химически связанных атомов двух или нескольких элементов. Состав химического соединения записывается в виде химических формул, а строение часто изображается структурными формулами.
Главная
Похожие презентации
 Для 8 класса "Простые вещества - неметалы"
Для 8 класса "Простые вещества - неметалы"
 Чистые вещества и смеси - Способы разделения смесей
Чистые вещества и смеси - Способы разделения смесей
 Чистые вещества и смеси
Чистые вещества и смеси
 Урок-смотр знаний по теме «Изменения, происходящие с веществами» 8 класс
Урок-смотр знаний по теме «Изменения, происходящие с веществами» 8 класс
 Обобщение сведений о некоторых газообразных веществах
Обобщение сведений о некоторых газообразных веществах
Поделиться ссылкой на презентацию через:
Код для вставки видеоплеера презентации на свой сайт:

