Текст этой презентации
Слайд 1

Презентация
Раздел: Органическая химия.
Аминокислоты
Слайд 2

Введение:
Аминокислоты – азотосодержащие
органические соединения, в молекулах которых содержатся аминогруппа -NH2
и карбоксильная группа -СООН Простейшим представителем является
аминоэтановая кислота H2N – CH2 - COOH
Слайд 3
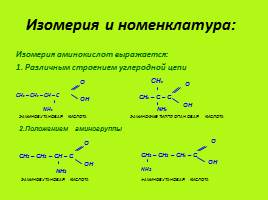
Изомерия и номенклатура:
Изомерия аминокислот выражается:
1. Различным строением углеродной цепи CH3 – CH2 – CH – C NH2
O
OH
CH2 – CH2 – CH2 – C NH2
4-АМИНОБУТАНОВАЯ КИСЛОТА
O
OH
2-АМИНОБУТАНОВАЯ КИСЛОТА
CH3 – C – C NH2
O
OH
сн3
2-АМИНО-2-МЕТИЛПРОПАНОВАЯ КИСЛОТА
CH3 – CH2 – CH – C NH2
O
OH
2-АМИНОБУТАНОВАЯ КИСЛОТА
2.Положением аминогруппы
Слайд 4

Получение:
Аминокислоты, входящие в состав белков, получают путем их гидролиза. Известны синтетические способы получения аминокислот. Например, в молекулах карбоновых кислот атомы водорода в радикале можно заменить на галоген, а галоген действием аммиака – на аминогруппу. Cl – CH2 – COOH + NH3 = NH2 – CH2 – COOH + H Cl
Аминокислоты можно получить из предельных углеводородов
C2H6 C2H5Cl C2H5OH CH3 - COOH CH2Cl - COOH NH2 – CH2 – COOH
Слайд 5

Физические свойства:
Аминокислоты – бесцветные
кристаллические вещества, хорошо
растворимые в воде. Многие из них обладают сладким вкусом.
Слайд 6

Химические свойства:
В молекулах аминокислот содержатся
карбоксильные группы, имеющие кислотные
свойства, и аминогруппы, обладающие
основными свойствами, т.е. аминокислоты являются амфотерными соединениями
1. Реакции по карбоксильной группе: а) взаимодействие с основаниями
H2N – CH2 – COOH + NaOH = Н2N – CH2 – COONa + H2O б) взаимодействие со спиртами
H2N – CH2 – COOH +НОR = H2N – CH2 – COOR +H2O
Слайд 7

Химические свойства:
2. Реакции по аминогруппе: а) взаимодействие с кислотами
НООС – СН2 – NH2 + HCl = HOOC – CH2 – NH3Cl 3. Особые свойства: а) взаимодействие друг с другом H2N – CH2 – COOH + H2N – CH2 – COOH =
= H2N – CH2 – CONН – CH2 – COOH Образовавшаяся молекула реагирует с другой такой же молекулой и получаются высокомолекулярные соединения.
Слайд 8

Химические свойства:
б) Наличие в молекуле одинакового числа аминогрупп и
карбоксильных групп приводит к взаимной внутренней
нейтрализации. H – N – CH2 – C H – N – CH2 – COO Полученная соль имеет два противоположных заряда и
называется биполярным ионом. Ее раствор нейтрален
o
O-H
H
H
Слайд 9

Применение:
1. Аминокислоты необходимы для синтеза белков в живых
организмах.
2. В медицинских целях.
3. Для подкормки животных.
4. Для синтеза некоторых волокон ( например, капрона ).
 Химия металлов
Химия металлов
 Формирование универсальных учебных действий на уроках химии
Формирование универсальных учебных действий на уроках химии
 Углеводы
Углеводы
 Коррозия металлов и способы защиты от коррозии
Коррозия металлов и способы защиты от коррозии
 Соли
Соли










